Una de las maneras de incrementar la temperatura de un cuerpo es colocarlo en contacto con otro cuerpo más CALIENTE.
La energía térmica (CALOR) del
cuerpo más caliente disminuye y la del cuerpo más frío aumenta,
presentándose una transferencia de CALOR como resultado de la diferencia de TEMPERATURA.
Como conclusión
podemos decir que el CALOR es la
energía transferida de un cuerpo a otro debido a la diferencia de TEMPERATURA. Para representar el calor usaremos el símbolo Q.
Veamos algunos videos donde se puede observar el calor específico del agua.
Video uno
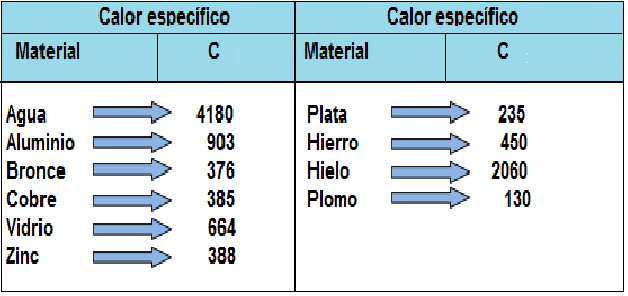
El calor específico (C) se emplea para determinar la cantidad de calor (Q) que debe transferirse para cambiar en cierta cantidad la temperatura de una masa dada. A continuación veremos el calor específico de algunas sustancias:
El calor Q fluye espontáneamente de un cuerpo
más caliente a uno más frío.
Calor específico
El calor específico de una sustancia determinada
se define como el incremento de su ENERGÍA
TÉRMICA cuando un kilogramo de la sustancia aumenta su temperatura en un
grado KELVIN. El calor específico se
representa por el símbolo C y se
mide en:
Joule
C =
-----------------------
Kg
x °K
Veamos algunos videos donde se puede observar el calor específico del agua.
Video uno
Video dos
Video tres
Vídeo cuatro: Razones por la q no se debe mezclar agua con aceite caliente.
El calor específico (C) se emplea para determinar la cantidad de calor (Q) que debe transferirse para cambiar en cierta cantidad la temperatura de una masa dada. A continuación veremos el calor específico de algunas sustancias:
El CALOR ganado o perdido por un cuerpo cuando cambia su TEMPERATURA, depende de su masa,
del cambio de la temperatura y del calor específico del cuerpo, es decir:
Ejemplo
Un bloque de plomo de 0,800 Kg de masa se calienta desde los 210 °K hasta 300°K. Halle el Q que absorvio el PLOMO.
Experimento de energía térmica Experimento de energía calórica Calor específico, ejercicio