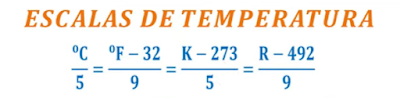lunes, 23 de marzo de 2015
sábado, 28 de febrero de 2015
Termodinámica: Historia
Entre los años 1600 y 1700, Europa vivió
una etapa de mucho
frio, por lo
tanto los científicos de la época se vieron obligados a estudiar el ¨CALOR¨,
dando como resultado la invención de máquinas que fueron utilizadas para
eliminar el intenso frío y así poder independizarse del calor
proporcionado tanto por el ser humano como por los
animales. Más adelante estas máquinas mejoraron y fue así como surgió la ciencia de la termodinámica.
Termodinámica viene del griego “termo” que significa “calor” y “dinámico” que significa “fuerza” y describe cómo
los sistemas macroscópicos responden a los cambios en su entorno.
Históricamente, la termodinámica se desarrolló a partir de la necesidad de
aumentar la eficiencia de las primeras máquinas de vapor. En esencia,
estudia la circulación de la energía y cómo ésta infunde movimiento a
partir de la temperatura,
presión y volumen e incluye una magnitud llamada Entropía, que mide el orden y el estado dinámico de los sistemas.
Se entiende por termodinámica a la parte de la física que
describe y relaciona las propiedades de la materia,
así como sus intercambios energéticos. En otras palabras
podemos decir que termodinámica es
el estudio de las propiedades de la energía térmica y de sus cambios.
 En el siglo XVIII los científicos empezaron a entender la diferencia entre un
cuerpo caliente y uno frío, dando explicaciones como que
cuando un cuerpo se calentaba aparecía una sustancia
invisible que llamaron ¨Calórico¨. Decían que los cuerpos calientes,
tenían más ¨Calórico¨ que los cuerpos
fríos, sin embargo esta teoría no podía explicar todo. Es por eso que a finales
del siglo XIX apareció una nueva teoría que remplazaría a la del ¨Calórico¨. Esta nueva teoría decía que la materia estaba constituida por pequeñas partículas que se mueven constantemente, con la diferencia de que en un cuerpo CALIENTE las partículas se mueven más rápido, por lo tanto tendrán mayor ENERGÍA que las partículas del
cuerpo FRÍO. A esta teoría la llamaron TEORÍA CINÉTICA MOLECULAR.
En el siglo XVIII los científicos empezaron a entender la diferencia entre un
cuerpo caliente y uno frío, dando explicaciones como que
cuando un cuerpo se calentaba aparecía una sustancia
invisible que llamaron ¨Calórico¨. Decían que los cuerpos calientes,
tenían más ¨Calórico¨ que los cuerpos
fríos, sin embargo esta teoría no podía explicar todo. Es por eso que a finales
del siglo XIX apareció una nueva teoría que remplazaría a la del ¨Calórico¨. Esta nueva teoría decía que la materia estaba constituida por pequeñas partículas que se mueven constantemente, con la diferencia de que en un cuerpo CALIENTE las partículas se mueven más rápido, por lo tanto tendrán mayor ENERGÍA que las partículas del
cuerpo FRÍO. A esta teoría la llamaron TEORÍA CINÉTICA MOLECULAR.
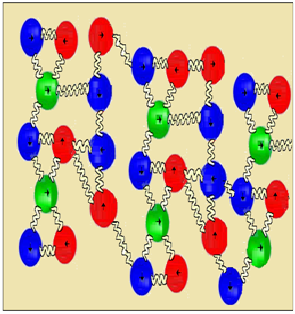
Para entender mejor lo que
sucede con la teoría cinética molecular,
usaremos un ejemplo sencillo cuando se lanza una pelota.
De la gráfica anterior se puede observar que el cuerpo posee una energía cinética en virtud de su velocidad y una energía potencial en virtud de su altura. Estas energías hacen parte de la energía total externa, sin embargo las partículas internas que conforman la pelota están en constante movimiento, por lo tanto también poseen energía potencial y cinética.
Sí amplificamos una parte
de la pelota, las partículas internas también
están en constante movimiento, éstas están unidas unas a otras por medio de una
especie de ¨resorte¨ que a su vez
posee energía potencial elástica y energía cinética, el resorte hace las
veces de las fuerzas electromagnéticas
que mantienen unida a la pelota.
La suma de las energías cinética
y potencial de todo el movimiento interno de las
partículas se llamará ENERGÍA TÉRMICA o energía interna.
Máquina de vapor Máquina de vapor II Máquina de vapor III Termodinámica Sistemas termodinámicos Teoría cinética molecular TCM II, animación
Temperatura
La temperatura y nuestros
sentidos. Equilibrio térmico.
¿Qué es lo
que queremos hacer?
Solemos asociar la temperatura con la sensación física de "frío" o la de "calor".
Estas ideas son totalmente subjetivas, según el sentido en que la energía se transfiera de un sistema a
otro. Además puede suceder que un
sistema que transfiere energía
no experimente cambio de temperatura
alguno.
¿Qué nos
hará falta?
¿Cómo lo
haremos?
Muchas veces hemos observado
algunos cuerpos en los que se transmite el calor
por medio del contacto. Este fenómeno se debe a una diferencia entre los
cuerpos. Te has hecho la pregunta ¿Cuál es esa diferencia?
Después sumergir tus manos
en los recipientes:
¿Qué sientes, frío, calor o ambas cosas?
Ante un mismo estímulo, ¿Se siente la misma sensación?
Los receptores de temperatura del organismo ¿Son
buenos medidores o dependen de otras variables?
¿Conoces algún sistema para medir la temperatura fielmente que no se deje engañar como la mano?
El resultado
obtenido es..............que "la temperatura de un sistema es la propiedad que determina si un sistema se encuentra o
no en equilibrio térmico con otros
sistemas".
Los
términos "se enfría" y "se calienta" conviene
relacionarlos únicamente con la temperatura,
que es un índice del nivel de energía del cuerpo (energía interna). Esta si se puede poseer. Un sistema, al perder energía
interna, pierde temperatura,
"se enfría", y al ganar
energía interna "se calienta".
El equilibrio térmico, o más apropiadamente, el equilibrio
energético es la situación final a la que llegan dos cuerpos cuando se
ponen en contacto, estos cuerpos disponen inicialmente de temperaturas
diferentes.
La energía pasa
en forma de calor desde el cuerpo caliente al cuerpo frío, hasta llegar a un equilibrio energético en que no hay
intercambio de calor (principio cero de
la termodinámica).
jueves, 26 de febrero de 2015
Transferencia de energía
Energía térmica
La energía térmica se puede transferir o
propagar de una región a otra en el mismo cuerpo o de un cuerpo a otro. Esta transferencia de energía se puede dar de tres formas diferentes: Conducción, convección y por radiación.
Guía
didáctica Conducción calórica
Institución:
Docentes:
Luis Fernando Posada M.
Área:
Ciencias
naturales Grado: 10º 11°
Asignatura:
Física
Objetivo:
Describir cualitativamente
el proceso para hacer que el calor se transmita de un cuerpo a otro por medio del contacto. Demostrar experimentalmente
que el papel no se quemará aunque se ponga directamente al fuego, sin importar cuánto tiempo dure la experiencia.
Para realizar la
siguiente actividad, es necesario tener los siguientes materiales: Papel, caja o paralelepípedo sin tapa, fósforos, mechero
o fuente de calor, moneda, clavo, un cigarrillo, globos y agua.
Se debe preparar un
recipiente de papel que nos sirva después de caja. Una vez construido la caja
de papel, la pondremos sobre el soporte o mechero, la llenaremos de agua y podremos prender el fuego. Observa que pasa.
¿Crees que la caja con agua cambiará su forma? ¿Por qué?
¿Qué pasará si la caja se coloca en el mechero sin agua?
Compara ambos resultados. ¿Qué
explicación física encuentras?
El contacto con el agua hace que el calor se
transmita del papel al agua y que, en consecuencia, la temperatura del papel no llegue a la de su inflamación. Obviamente,
si no hubiera agua, todo el calor
dado por el fuego se destinaría a aumentar la energía interna del papel y a incrementar su temperatura hasta
hacerlo arder.
Otra experiencia
similar que puedes verificar es cuando se acercan las brasas de un cigarrillo a
un papel que esté justamente en contacto
con una moneda. Observa muy bien.
¿Qué sucede con el papel?
¿Qué le pasa a la moneda?
¿El calor se propaga? Averígualo y contesta.
¿Qué fenómeno físico se
presenta? Piensa.
Igualmente ocurre si enrollamos fuertemente un papel
alrededor de un clavo o cualquier objeto metálico: al ponerlo al fuego, el
papel no arderá. Investígalo.
Es la transferencia de energía cinética entre las partículas de un cuerpo cuando
estas chocan. La conducción es la
transferencia de energía térmica más común en los sólidos.
Conducción I Conducción II
Conducción I Conducción II
Convección
Es la transferencia de calor
en un fluido a través del movimiento del propio fluido. Este movimiento
de los fluidos se debe a la diferencia
de densidad y de temperatura.
Otro
ejemplo de la convección es el que se
observa en el aire que circula dentro de
una habitación.
Convección, animación. Convección II
Convección, animación. Convección II
Es la transferencia de energía térmica a través del espacio en forma de ondas
electromagnéticas. El ejemplo más claro de la radiacción, se observa en la energía solar que llega
a la tierra.
Radiacción. ¿Qué es? Transferencia de calor ¿Qué es el calor? Calor y temperatura
Radiacción. ¿Qué es? Transferencia de calor ¿Qué es el calor? Calor y temperatura
Hemos hablado del calor y
la temperatura. El calor y la temperatura, aunque están muy
relacionados no tienen el mismo
significado.
Calor ¿Qué es?
 El calor es una forma de energía y se puede medir en Julios
o en Ergios. En otras palabras
podemos decir que calor es la energía que se necesita para poner en
agitación todas las moléculas del cuerpo.
El calor es una forma de energía y se puede medir en Julios
o en Ergios. En otras palabras
podemos decir que calor es la energía que se necesita para poner en
agitación todas las moléculas del cuerpo.
El calor es la sensación que se percibe
gracias a la variación de la temperatura. El calor de un cuerpo depende de su MASA.
Temperatura ¿Qué es?
La
temperatura se define como el nivel de
calor o nivel calórico de un cuerpo. En otras palabras la temperatura
de un cuerpo tiene que ver con la energía
cinética de sus moléculas.
Dos
cuerpos pueden tener la misma TEMPERATURA
y distinta cantidad de CALOR. Por
ejemplo sí se hierve agua en dos recipientes diferentes, ambos alcanzan una
temperatura de 100 °C, pero el
recipiente que tiene más agua,
encierra mayor cantidad de calor.
Sí se ponen en contacto dos cuerpos que tienen diferente TEMPERATURA, el más CALIENTE pierde energía térmica (interna), la cual a su vez es absorbida por el cuerpo más FRÍO, cuya energía interna aumenta. En este caso se puede observar la aplicación de la ley de conservación de la energía, ya que la energía que pierde
el cuerpo CALIENTE, la gana el cuerpo FRÍO.
En la
gráfica anterior se puede
observar que las partículas del cuerpo caliente
tienen mayor ENERGÍA CINÉTICA (Mayor velocidad) que las partículas del cuerpo frío, cuando se ponen en contacto los
dos cuerpos, la velocidad de las partículas en ambos cuerpos es la misma.
Dos cuerpos de distinta MASA
que estén igual de calientes tienen la
misma TEMPERATURA (Nivel de calor),
aunque el de mayor masa encierra más cantidad de CALOR (Energía).
De todo lo anterior se
puede decir que la TEMPERATURA no
depende de la masa del cuerpo, en cambio la energía térmica (CALOR) sí depende de la masa.
Equilibrio térmico
 Dos cuerpos están en equilibrio térmico
cuando tienen la misma temperatura. Este equilibrio se puede observar cuando a un
cuerpo CALIENTE se le acerca un
cuerpo más FRÍO (por ejemplo un termómetro), se
presenta entonces un choque entre las partículas del cuerpo caliente y las
partículas del cuerpo frío, dándose una transferencia
de energía del cuerpo caliente al frío, hasta lograr que ambos cuerpos
tengan la misma temperatura.
Dos cuerpos están en equilibrio térmico
cuando tienen la misma temperatura. Este equilibrio se puede observar cuando a un
cuerpo CALIENTE se le acerca un
cuerpo más FRÍO (por ejemplo un termómetro), se
presenta entonces un choque entre las partículas del cuerpo caliente y las
partículas del cuerpo frío, dándose una transferencia
de energía del cuerpo caliente al frío, hasta lograr que ambos cuerpos
tengan la misma temperatura.
Escalas de temperatura
Antes de hablar de
escalas de medición, es necesario definir el concepto de TERMÓMETRO. Un termómetro
es un instrumento que se utiliza para medir la temperatura de un cuerpo determinado. El termómetro se coloca en
contacto con el cuerpo hasta lograr un EQUILIBRIO TÉRMICO.
Existen diferentes escalas de
medición de la temperatura, estas fueron creadas por los científicos para
poderlas comparar entre sí. Entre
las principales escalas de temperatura tenemos: La escala Celsius, la escala Kelvin
y la escala Fahrenheit.
Escala Celsius
Fue creada por el astrónomo y físico sueco Anders Celsius, esta escala se
creó con
base en las propiedades del agua. En esta escala el punto de congelación (FUSIÓN) del agua pura es a
los 0°C y el punto de EBULLICIÓN del agua pura es a los 100 °C, además la temperatura del
cuerpo humano es a los 37 °C.
Escala Kelvin
En esta escala el punto
de FUSIÓN (Congelación del
agua) es a los 273 °K y el punto de EBULLICIÓN del agua es a los 373 °K. Cabe recordar que la
escala KELVIN se basa en el cero
absoluto. La temperatura del cuerpo humano se da a los 310 °K.
Escala Fahrenheit
En esta
escala
el punto de FUSIÓN (Congelación del agua) es a los 32
°F y el punto de EBULLICIÓN del agua es a los 212 °F. La temperatura del
cuerpo humano se da a los 98 °F.
Para establecer equivalencias entre las distintas escalas se tomó como referencia los puntos de FUSIÓN y EBULLICIÓN
del agua a presión atmosférica normal.
Según
las escalas anteriores se puede establecer una relación entre ellas para pasar
de grados Celsius a Kelvin o Fahrenheit,
así:
Veamos la temperatura de algunos planetas de nuestro sistema solar:
Suscribirse a:
Comentarios (Atom)